Radioterapia aumenta riesgo de cáncer de mama en jóvenes
Por el equipo editorial de MedImaging en español
Actualizado el 19 Nov 2013
Exponer a las mujeres jóvenes y a las niñas menores de 20 años a radiación ionizante puede aumentar el riesgo de cáncer de mama más tarde en la vida. Los científicos pueden ahora haber encontrado la respuesta a por qué esto ocurre. Los hallazgos de un estudio colaborativo apuntaron a un aumento de la auto-renovación de las células madre y el enriquecimiento consecuente de las células madre mamarias, como la razón.Actualizado el 19 Nov 2013
Las mamas con células madre mamarias como resultado de la radiación ionizante durante la pubertad muestra una tendencia a desarrollar tumores negativos para los receptores de estrógeno (RE). Los receptores de estrógenos, por ej., proteínas activadas por la hormona estrogénica, son vitales para el desarrollo normal de la mama y otras características sexuales femeninas durante la pubertad.
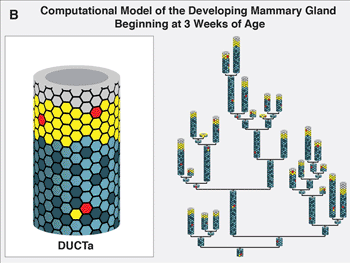
Imagen: Un modelo de computación de la glándula mamaria en desarrollo empezando a las tres semanas de edad (Fotografía cortesía de la División de Ciencias Biológicas del Laboratorio Nacional Lawrence Berkeley del Departamento de Energía de los Estado Unidos).
“Nuestros resultados están de acuerdo con los estudios de epidemiología que muestran que los cánceres de mama, humanos, inducidos por radiación tienen más probabilidad de ser RE negativos que son cánceres de mama espontáneos”, dijo la Dra. Sylvain Costes, una biofísica de la División de Ciencias Biológicas del Laboratorio Lawrence Berkeley (LBL; Berkeley, CA, EUA; www.lbl.gov/lsd) del Departamento de Energía (DOE) de los Estados Unidos. “Esto es importante porque los cánceres de mama RE-negativos son menos diferenciados, más agresivos, y con frecuencia, tienen un peor pronóstico en comparación con los otros subtipos de cáncer de seno”.
Los Dres. Costes y Jonathan Tang, también de la División de Ciencias Biológicas del Laboratorio Berkeley, fueron parte de una colaboración liderada por la Dra. Mary Helen Barcellos-Hoff, anteriormente del Laboratorio Berkeley y ahora de la Facultad de Medicina de la Universidad de Nueva York (Nueva York, NY, EUA), quien estudió la tan llamada “ventana de susceptibilidad” que se sabe existe entre los tratamientos de radiación en la pubertad y el riesgo de cáncer de mama en la edad adulta tardía. La clave de su éxito fueron modelos basados en dos linajes mamarios (ABMs) que desarrollaron, en los cuales un sistema es modelado como una recolección de unidades de toma de decisión autónoma llamadas agentes. Una ABM simuló los efectos de la radiación sobre la glándula mamaria durante las etapas de desarrollo o durante la edad adulta. La otra simuló la dinámica de crecimiento de las células epiteliales mamarias humanas en crecimiento en cultivo después de la irradiación.
“Nuestra ABM de glándula mamaria consistió de millones de agentes, con cada agente representando una célula madre mamaria, una célula progenitora o una célula diferenciada en la mama”, declaró el Dr. Tang. “Corrimos miles de simulaciones en el supercomputador Lawrencium del Laboratorio Berkeley durante el cual cada agente evaluó continuamente su situación y tomo decisiones con base en una serie de reglas que corresponden a propiedades biológicas conocidas o hipotéticas de las células mamarias. La ventaja de este método es que nos permite ver las consecuencias globales para el sistema que emergen en el tiempo desde nuestras asunciones acerca de agentes individuales. Para nuestro conocimiento, nuestro modelo de glándula mamaria es el primer modelo a escala del desarrollo de las glándulas enteras desde el inicio de la pubertad hasta la edad adulta”.
La investigación epidemiológica ha demostrado que las niñas de menos de 20 años, a las que se les administran tratamientos de radioterapia para enfermedades como el linfoma de Hodgkin tienen cerca del mismo riesgo de desarrollar cáncer de seno en sus 40s como las mujeres que nacieron con una mutación del gen BRCA. De su estudio, los Dres. Costes, Tang, y sus colegas, concluyeron que la auto-renovación de las células madre fue probablemente el principal proceso responsable.
“La auto-renovación de la célula madre fue el único mecanismo en el modelo de la glándula mamaria que llevó a las predicciones que fueran consistentes con los datos de nuestro trabajo in vivo en ratones y nuestros experimentos in vitro con MCF10A, una línea celular epitelial mamaria humana”, anotó el Dr. Tang. “Adicionalmente, nuestro modelo predice que este mecanismo solo generaría más células madre durante la pubertad mientras que la glándula se está desarrollando y está sucediendo una proliferación celular considerable”.
Los investigadores ahora están buscando biomarcadores genéticos o fenotípicos que identificarían a las niñas jóvenes que están en riesgo mayor de cáncer de mama por la radioterapia. Los resultados del estudio de la Dra. Barcellos-Hoff y su grupo de investigación muestran asociaciones entre la radiación ionizante y el cáncer de mama que se extienden más allá del daño al ADN y las mutaciones.
“Esencialmente, la exposición del seno a la radiación ionizante genera una señal bioquímica general que le dice al sistema que algo malo sucedió”, dijo el Dr. Costes. “Si la exposición tiene lugar durante la pubertad, esta señal dispara la respuesta regenerativa llevando a un “grupo” más grande de células madre, aumentando por lo tanto la probabilidad de desarrollar cánceres de seno agresivos ER-negativos, más tarde en la vida”.
Los hallazgos de este estudio colaborativo fueron publicados en línea en la revista Stem Cells.
Enlace relacionado:
Lawrence Berkeley US National Lab’s Life Sciences Division