Nuevo anticuerpo radiomarcado mejora el diagnóstico y tratamiento de tumores sólidos
Actualizado el 06 May 2025
El receptor de interleucina-13 α-2 (IL13Rα2) es un receptor de superficie celular que se encuentra comúnmente en tumores sólidos como el glioblastoma, el melanoma y el cáncer de mama. Su expresión es mínima en tejidos normales, lo que lo convierte en una diana ideal para la detección no invasiva y específica de tumores. Sin embargo, a pesar de su potencial, actualmente no existen anticuerpos dirigidos contra IL13Rα2 para uso diagnóstico o terapéutico (teranóstico) en entornos clínicos.
Un anticuerpo radiomarcado recientemente desarrollado, dirigido al antígeno canceroso IL13Rα2, ha demostrado una alta especificidad, uniéndose exclusivamente a las células cancerosas y evitando la interacción con el antígeno relacionado IL13Rα1, que se expresa más ampliamente en tejidos sanos. Al probarse en varios tipos de cáncer, el anticuerpo radiomarcado fue eficaz para identificar tumores con una dosis masiva inyectada baja, lo que sugiere su potencial para aplicaciones de radioinmunoterapia.
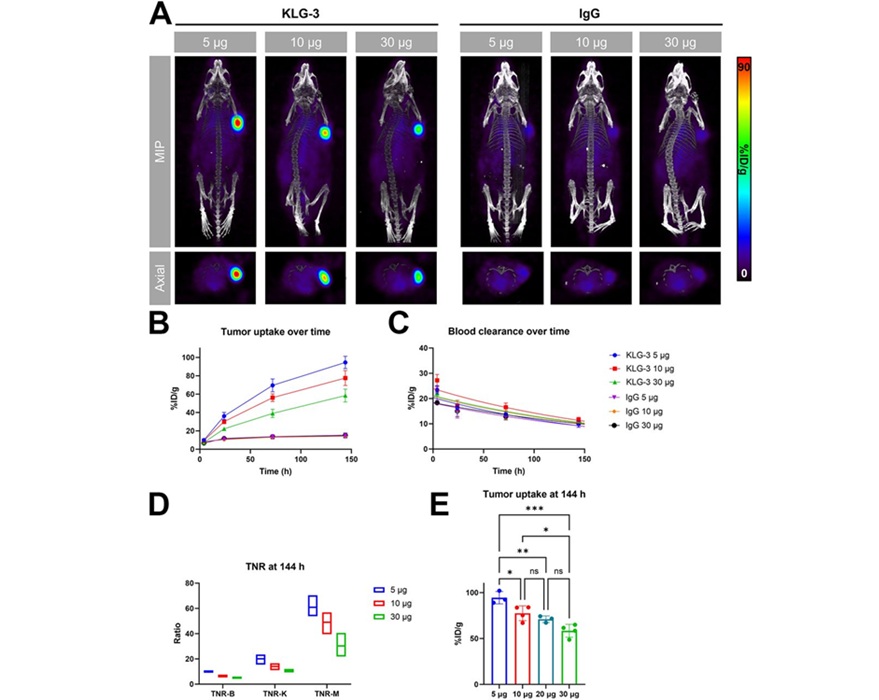
En un estudio publicado en The Journal of Nuclear Medicine, investigadores del MD Anderson Cancer Center de la Universidad de Texas (Houston, Texas) desarrollaron cinco nuevos anticuerpos humanos anti-IL13Rα2 (KLG-1 a KLG-5). El equipo evaluó las propiedades de unión y la especificidad del objetivo de estos anticuerpos in vitro, y realizó imágenes in vivo de 89Zr-inmuno-PET en un modelo de ratón de glioblastoma.
Tras la selección de KLG-3 como el candidato más prometedor, los investigadores llevaron a cabo un estudio de titulación de dosis masiva. El análisis de biodistribución ex vivo se utilizó para determinar la dosimetría efectiva de la terapia con KLG-3 marcado con 177Lu. La efectividad de la focalización de KLG-3 también fue evaluada en un modelo murino de melanoma.
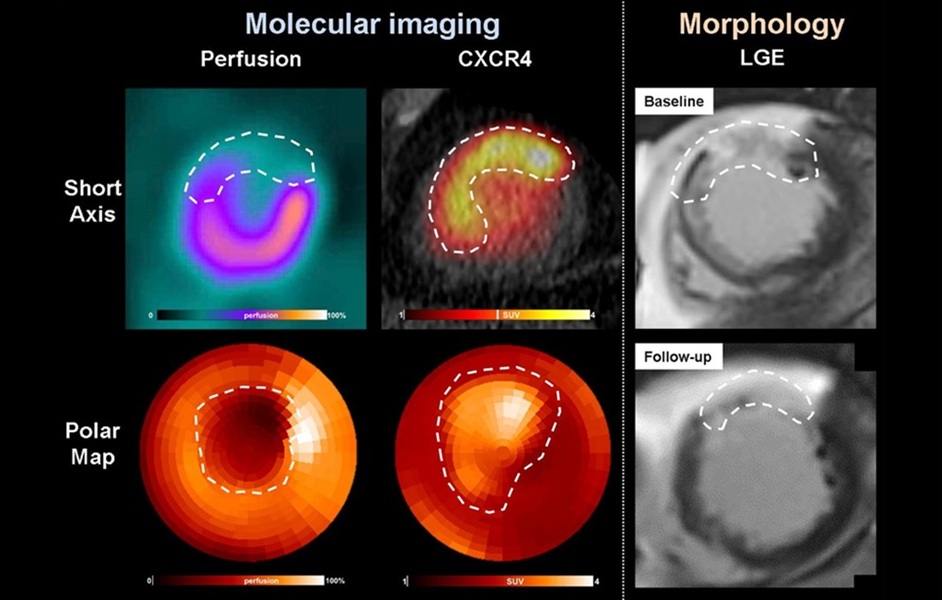
El anticuerpo principal, KLG-3, demostró una unión altamente específica a dianas en modelos humanos de glioblastoma y melanoma, generando imágenes PET de alto contraste con mínima acumulación de material fuera del objetivo en tejidos sanos. La dosimetría prospectiva del KLG-3 marcado con 177Lu indicó potencial terapéutico a dosis inyectadas relativamente bajas, lo que proporciona evidencia sólida que respalda el desarrollo continuo de KLG-3 para su uso en radioinmunoterapia.
“Estos resultados demuestran un avance significativo en el uso de IL13Rα2 como diana viable en la terapia contra el cáncer. La implementación de las moléculas diana desarrolladas en este estudio podría dar lugar a fármacos dirigidos a tumores altamente específicos y eficaces, con escasos efectos secundarios para los pacientes”, afirmó la Dra. Simone Krebs, profesora asociada del Centro Oncológico MD Anderson de la Universidad de Texas.
“Se sabe que IL13Rα2 es un precursor de la inmunosupresión y, por lo tanto, la inmuno-PET dirigida a IL13Rα2 podría identificar este fenotipo molecular, lo que podría facilitar la selección de pacientes y comprender quiénes podrían beneficiarse de las estrategias combinatorias”.