PET personaliza tratamiento para el cáncer
|
Por el equipo editorial de MedImaging en español Actualizado el 28 Mar 2018 |
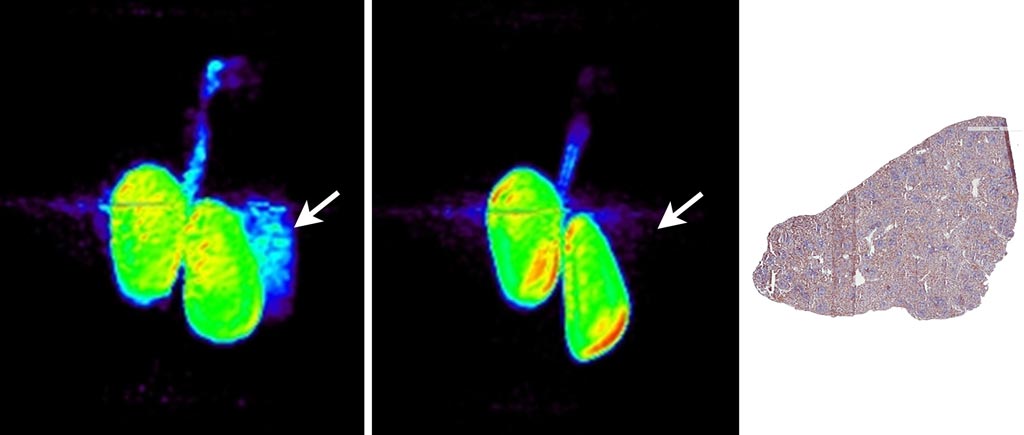
Imagen: PET de los riñones y el bazo 90 minutos después de la inyección de 18F-BMS-986192 y de la inmunohistoquímica anti-PD-L1 del tejido sano del bazo de un mono (R) (Fotografía cortesía de David Donnelly/BMS).
Un método de imagenología no invasivo, basado en la tomografía por emisión de positrones (PET) del mismo día, podría ayudar a orientar las decisiones de tratamiento del cáncer y evaluar la respuesta al tratamiento, según un nuevo estudio.
Investigadores de Bristol-Myers Squibb (BMS, Princeton, NJ, EUA) han desarrollado una proteína diseñada, etiquetada con flúor-18 (18F) contra la proteína de la muerte programada (PD-1) y su ligando PD -L1, una proteína y que permite que el cáncer evada el sistema inmune. El radioligando PD-L1 (18F-BMS-986192) se evaluó luego en ratones con tumores subcutáneos PD-L1(-) y PD-L1(+) bilaterales en tejidos humanos, así como en la distribución, unión y dosimetría de radiación en monos cangrejeros sanos.
Los resultados revelaron que 18F-BMS-986192 se unió a los tejidos tumorales PD-L1 humanos y de los monos en función de la expresión de PD-L1, bloqueando la unión del radioligando de una manera dependiente de la dosis. Las imágenes de PET in vivo visualizaron claramente la expresión de PD-L1 en los ratones implantados con tumores de xenoinjerto PD-L1(+). Dos horas después de la dosificación, se observó una captación 3,5 veces mayor en los ratones implantados, en comparación con los ratones control con tumores PD-L1(-). La coadministración de una adnectina anti-PD-L1 redujo la captación tumoral a las dos horas después de la inyección en aproximadamente un 70%, lo que demuestra la unión específica de PD-L1.
La biodistribución en el mono cangrejero mostró unión en el bazo, que es rica en PD-L1, con eliminación rápida de la sangre a través de los riñones y la vejiga. La unión de PD-L1(+) en el bazo también se redujo mediante la administración conjunta de 18F-BMS-986192. Según los investigadores, los resultados demuestran la viabilidad del método, y que las estimaciones de dosimetría de radiación indican que el marcador es seguro de administrar en estudios en humanos. El estudio fue publicado en la edición de marzo de 2018 de la revista The Journal of Nuclear Medicine.
“Este método representa una oportunidad para que los médicos evalúen de forma no invasiva todos los tumores de un paciente para la expresión de PD-L1 con una sola PET y la lectura oportuna”, dijo el autor principal David Donnelly, PhD, de BMS Pharmaceutical Research and Development. “Esto puede ayudar a guiar las decisiones de tratamiento y a evaluar la respuesta al tratamiento, para ayudar a identificar el tratamiento adecuado para el paciente adecuado en el momento correcto y con la dosis correcta”.
La vía PD-1 es un receptor de la superficie celular que desempeña un papel importante en la regulación a la baja del sistema inmune y promueve la auto tolerancia al suprimir la actividad inflamatoria de las células T. La vía protege contra la autoinmunidad a través de un mecanismo dual para promover la apoptosis en las células T específicas de antígenos de los ganglios linfáticos, mientras que simultáneamente reduce la apoptosis en las células T reguladoras. A través de estos mecanismos, PD-1 inhibe el sistema inmune, previniendo enfermedades autoinmunes, pero también puede evitar que el sistema inmune mate a las células cancerosas.
Investigadores de Bristol-Myers Squibb (BMS, Princeton, NJ, EUA) han desarrollado una proteína diseñada, etiquetada con flúor-18 (18F) contra la proteína de la muerte programada (PD-1) y su ligando PD -L1, una proteína y que permite que el cáncer evada el sistema inmune. El radioligando PD-L1 (18F-BMS-986192) se evaluó luego en ratones con tumores subcutáneos PD-L1(-) y PD-L1(+) bilaterales en tejidos humanos, así como en la distribución, unión y dosimetría de radiación en monos cangrejeros sanos.
Los resultados revelaron que 18F-BMS-986192 se unió a los tejidos tumorales PD-L1 humanos y de los monos en función de la expresión de PD-L1, bloqueando la unión del radioligando de una manera dependiente de la dosis. Las imágenes de PET in vivo visualizaron claramente la expresión de PD-L1 en los ratones implantados con tumores de xenoinjerto PD-L1(+). Dos horas después de la dosificación, se observó una captación 3,5 veces mayor en los ratones implantados, en comparación con los ratones control con tumores PD-L1(-). La coadministración de una adnectina anti-PD-L1 redujo la captación tumoral a las dos horas después de la inyección en aproximadamente un 70%, lo que demuestra la unión específica de PD-L1.
La biodistribución en el mono cangrejero mostró unión en el bazo, que es rica en PD-L1, con eliminación rápida de la sangre a través de los riñones y la vejiga. La unión de PD-L1(+) en el bazo también se redujo mediante la administración conjunta de 18F-BMS-986192. Según los investigadores, los resultados demuestran la viabilidad del método, y que las estimaciones de dosimetría de radiación indican que el marcador es seguro de administrar en estudios en humanos. El estudio fue publicado en la edición de marzo de 2018 de la revista The Journal of Nuclear Medicine.
“Este método representa una oportunidad para que los médicos evalúen de forma no invasiva todos los tumores de un paciente para la expresión de PD-L1 con una sola PET y la lectura oportuna”, dijo el autor principal David Donnelly, PhD, de BMS Pharmaceutical Research and Development. “Esto puede ayudar a guiar las decisiones de tratamiento y a evaluar la respuesta al tratamiento, para ayudar a identificar el tratamiento adecuado para el paciente adecuado en el momento correcto y con la dosis correcta”.
La vía PD-1 es un receptor de la superficie celular que desempeña un papel importante en la regulación a la baja del sistema inmune y promueve la auto tolerancia al suprimir la actividad inflamatoria de las células T. La vía protege contra la autoinmunidad a través de un mecanismo dual para promover la apoptosis en las células T específicas de antígenos de los ganglios linfáticos, mientras que simultáneamente reduce la apoptosis en las células T reguladoras. A través de estos mecanismos, PD-1 inhibe el sistema inmune, previniendo enfermedades autoinmunes, pero también puede evitar que el sistema inmune mate a las células cancerosas.
Últimas Medicina Nuclear noticias
- Sistema de IA detecta de forma automática y confiable amiloidosis cardíaca mediante imágenes de gammagrafía
- Adquisición temprana de PET FDG dinámica de 30 minutos podría reducir a la mitad tiempos de exploración pulmonar
- El nuevo sistema radioteranástico detecta y trata el cáncer de ovario de forma no invasiva
- Nuevo método para desencadenar y obtener imágenes de convulsiones para ayudar a guiar cirugía de epilepsia
- Cirugía radioguiada detecta y elimina con precisión ganglios linfáticos metastásicos en pacientes con cáncer de próstata
- Nuevo trazador PET detecta artritis inflamatoria antes de que aparezcan síntomas
- Nuevo trazador PET mejora detección de lesiones en cáncer medular de tiroides
- Terapia dirigida administra radiación directamente a las células en cánceres difíciles de tratar
- Nuevo trazador PET identifica de forma no invasiva mutación del gen del cáncer para diagnóstico más preciso
- Algoritmo predice recurrencia del cáncer de próstata en pacientes tratados con radioterapia
- Nuevo trazador de imágenes PET identifica de forma no invasiva mutación del gen del cáncer para diagnóstico más preciso
- Tecnología láser ultrarrápida podría mejorar tratamiento del cáncer
- Radioterapia de dosis baja demuestra potencial para tratamiento de insuficiencia cardíaca
- Nuevo radiotrazador PET ayuda a detectar de forma temprana y no invasiva la enfermedad inflamatoria intestinal
- Combinación de imágenes por resonancia magnética y PET con aminoácidos podría ayudar a tratar tumores cerebrales agresivos
- Técnica de imágenes médicas permite visualización precisa de bacterias dirigidas a tumores
Canales
Radiografía
ver canal
El sistema directo de imágenes de rayos X médicos basado en IA es un cambio de paradigma con respecto a radiografías digitales y TC convencionales
Un innovador sistema inteligente de imágenes de rayos X por tomosíntesis tiene como objetivo combinar a la perfección las capacidades de la radiografía digital (RD), la tomografía... Más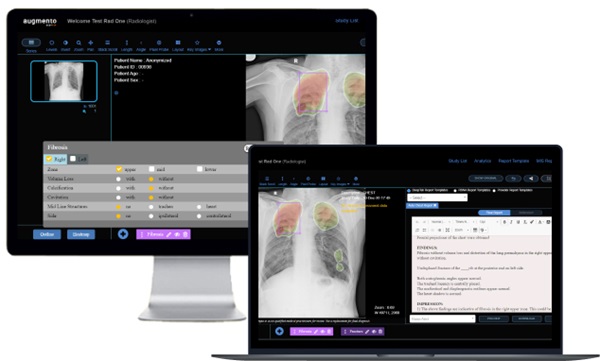
Solución de IA para rayos X de tórax identifica, categoriza y resalta automáticamente áreas sospechosas
La radiografía de tórax es la herramienta de imagen predominante empleada en las prácticas clínicas habituales y es crucial para detectar diversas enfermedades.... MásRM
ver canal
Exploración combinada PET-MRI mejora tratamiento para pacientes con cáncer de mama en etapa temprano
La ruta de diagnóstico típica para pacientes con cáncer de mama temprano a menudo implica mamografía, ecografía y, ocasionalmente, resonancias magnéticas.... Más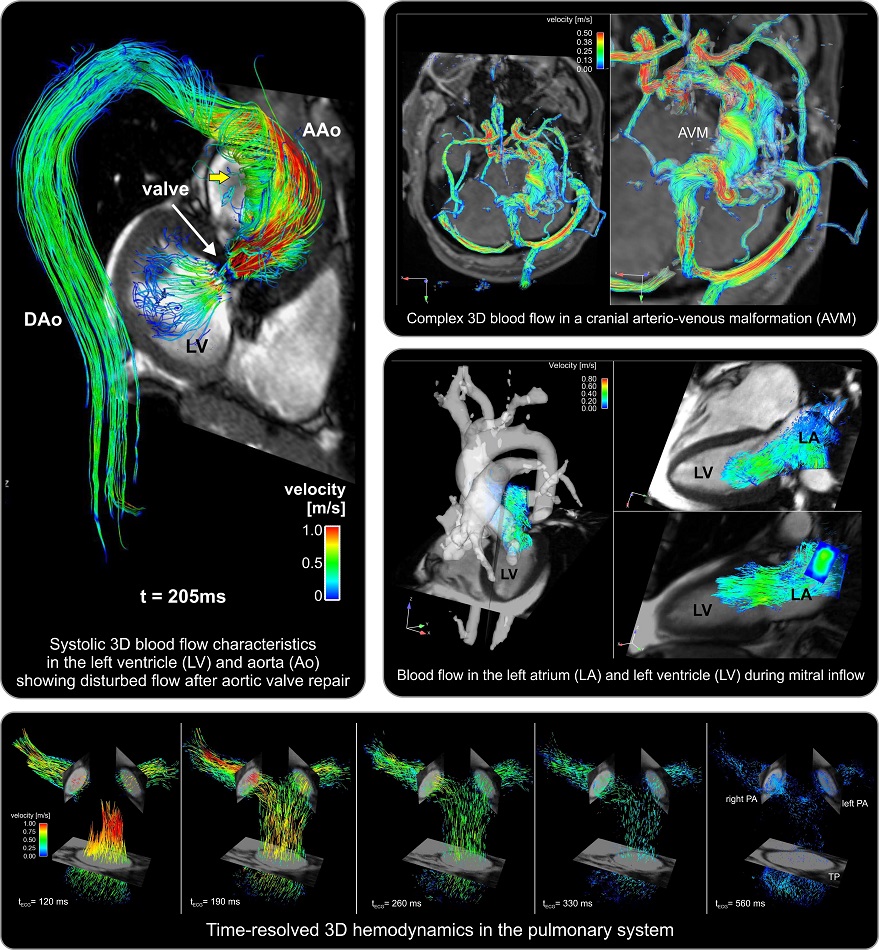
Resonancia magnética 4D podría mejorar evaluación clínica de anomalías del flujo sanguíneo del corazón
La resonancia magnética (RMN) utiliza imanes y radiofrecuencia pulsada para generar imágenes por computadora para detectar y diagnosticar afecciones médicas. La resonancia magnética... Más
Terapia de ultrasonido enfocado guiada por resonancia magnética se muestra prometedora en tratamiento del cáncer de próstata
Los médicos y radiólogos intervencionistas utilizan la terapia de ultrasonido enfocado guiado por resonancia magnética (MRgFUS) para apuntar con precisión áreas específicas... MásUltrasonido
ver canal
IA detecta COVID-19 en imágenes de ultrasonido pulmonar
Durante el inicio de la pandemia, utilizar inteligencia artificial (IA) para identificar signos de COVID-19 en imágenes de ultrasonido pulmonar resultó un desafío debido a los datos... MásNueva tecnología de ultrasonido podría revolucionar diagnóstico de enfermedades respiratorias
El tórax, ubicado entre el cuello y el abdomen, sirve como zona crítica para evaluar la salud respiratoria. Los médicos se basan en el análisis de las vibraciones sonoras creadas... MásImaginología General
ver canal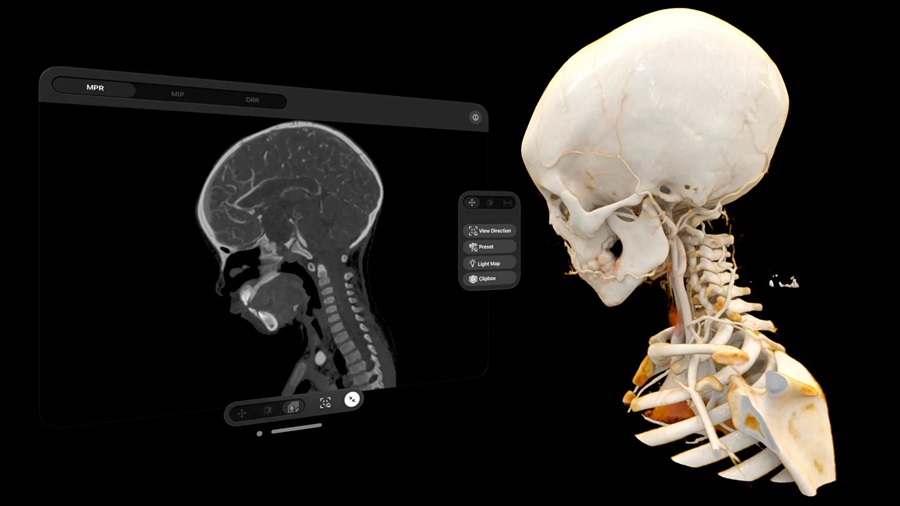
Aplicación RA convierte escaneos médicos en hologramas para ayudar en planificación quirúrgica
Siemens Healthineers (Erlangen, Alemania) ha lanzado una aplicación diseñada para Apple Vision Pro que permite a los usuarios, incluidos cirujanos, estudiantes de medicina o pacientes, ver... Más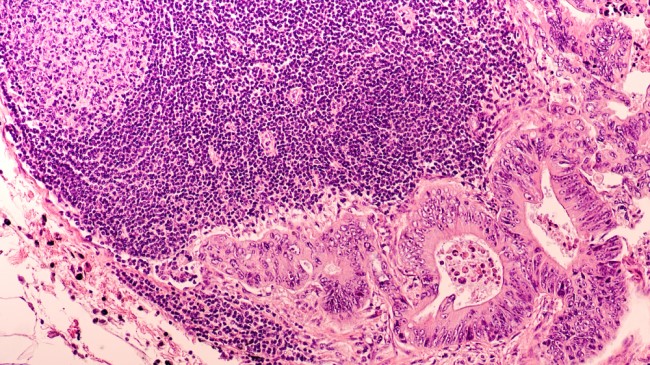
Tecnología de imágenes proporciona nuevo enfoque innovador para diagnosticar y tratar cáncer de intestino
Las biopsias, el método actual para diagnosticar el cáncer de intestino, son invasivas y conllevan riesgos como una posible infección. Si bien la medicina de precisión tiene... MásTI en Imaginología
ver canal
Nueva suite de imágenes médicas de Google Cloud hace los datos de imágenes médicas más accesibles
Las imágenes médicas son una herramienta fundamental que se utiliza para diagnosticar a los pacientes, y cada año se escanean miles de millones de imágenes médicas en... Más
Plataforma para el manejo de imágenes agiliza los planes de tratamiento
Un conjunto de soluciones de software del ecosistema de imágenes proporciona accesibilidad segura a las imágenes médicas, mejorando los flujos de trabajo y la atención a los pacientes. La plataforma... MásUna red global nueva mejora el acceso a la comprensión diagnóstica
Quest Diagnostics (Madison, NJ, EUA), un proveedor líder de servicios de información de diagnóstico, junto con otros proveedores de servicios de diagnóstico, ha anunciado la formación y el lanzamiento de la Red de Diagnóstico Global (GDN), un grupo de... Más
Una estación de trabajo nuevo apoya el flujo de trabajo de la imagenología pensando en los clientes
Una estación de trabajo de imagenología nueva ofrece una interfaz única e intuitiva para la toma eficiente de radiografías, fluoroscopias, mamografías y la toma de imágenes de las piernas/columna vertebral... MásIndustria
ver canal
Samsung y Bracco firman nuevo acuerdo de tecnología de ultrasonido de diagnóstico
Samsung Medison (Seúl, Corea del Sur) y Bracco Imaging (Milán, Italia) han firmado un Memorando de Entendimiento (MoU) para ser pioneros en una nueva área de dispositivos de diagnóstico... Más
IBA adquiere Radcal para ampliar oferta de garantía de calidad de imágenes médicas
Ion Beam Applications SA (IBA, Louvain-La-Neuve, Bélgica), líder mundial en tecnología de aceleradores de partículas y proveedor líder mundial de soluciones de dosimetría... Más
Sociedades internacionales sugieren consideraciones clave para herramientas IA para radiología
La inteligencia artificial (IA) tiene el potencial de alterar significativamente el campo de la radiología, presentando tanto oportunidades como desafíos. Su integración podría... Más